Уточняя причины развития патологического симптомокомплекса при наличии металлов в полости рта, Л.Д.Гожая (1988), Л.Д.Гожая, В.Н.Копейкин (1988), С.Т.Пырков (1990); I.Ruf (1989) и др. выделили три основных вида их патологического воздействия на организм: химико-токсическое, электрогальваническое и аллергическое. Есть специалисты [P.Koppenburg, M.Bacher, J.Geis-Gerstorter и др., 1987], которые скептически относятся к возможности токсического воздействия ионов металлов, высвобождающихся из металлических зубопротезных конструкций, так как определяемые ими величины концентраций металлов в смешанной слюне «не вызывали опасений».
Вместе с тем определение путей патологического воздействия металлов, имеющихся в полости рта, на организм привело к четкому разделению нозологических форм. Если заболевание обусловливается действием ионов тяжелых металлов, высвободившихся в слюну из зубопротезных конструкций, характеризуется появлением воспаления слизистой оболочки полости рта, а также обострением имеющихся ранее хронических воспалительных процессов в органах пищеварительного тракта, то оно трактуется как токсический стоматит. Если воспалительный процесс вызывается патогенным агентом (гаптеном) материала зубного протеза, хотя сам по себе агент может быть и нетоксичным или слаботоксичным, то говорят о возникновении аллергического стоматита, в основе которого лежит преимущественно гиперчувствительность замедленного типа [Л.Д.Гожая, 1988; Д.Л.Демнер, 1988; С.Т.Пырков, 1990].
В табл. 20 представлены основные различия между интоксикацией и аллергией на зубопротезные материалы.
В тех же случаях, когда специалисты не проводят четкой дифференциальной диагностики по механизму возникновения заболевания, обусловленного воздействием металлов в полости рта, то используют более универсальные термины: «гальванический синдром», «явления непереносимости к металлическим включениям в полости рта», «непереносимость организма к металлам» [С.Т.Пырков, 1990].
Практический интерес представляет исследование, проведенное С.Т.Пырковым (1990). При обследовании 100 больных с непереносимостью металлических зубных протезов (нержавеющая сталь; сталь, покрытая нитридом титана; сталь и золото) им было установлено, что у большинства из обследованных непереносимость была электрохимической природы и только у 8 — аллергической. Редкость возникновения аллергических реакций на слизистой оболочке полости рта объясняется ее анатомофизиологическими особенностями: слюноотделение, интенсивное всасывание, быстрое ферментативное разрушение и перестройка аллергенов, гематогенный транспорт (хорошая гемомикроциркуляция). Доказано, что для реализации аллергической реакции на слизистой оболочке полости рта требуется в 5-12 раз большая концентрация аллергенов, чем на коже [С.Т.Пырков, В.С.Погодин, Ю.С.Подкин, 1989; A.Lussi, 1987]. Вместе с тем ЛД.Гожая (1988) считает, что аллергические заболевания и реакции, обусловленные материалами зубных протезов, несколько выше. На основании стоматологического и аллергологаческого (накожные пробы, реакции специфической агломерации лейкоцитов, специфического подавления ретракции кровяного сгустка и тройного розеткообразования) методов обследования 584 человек с первичным диагнозом «непереносимость зубных протезов» она диагностировала аллергический стоматит в 30,3% случаев, а именно у 177 человек, причем у 88 из них стоматит был обусловлен аллергией к металлам.
Таблица 20.
Различия между интоксикацией и аллергией на материалы зубных протезов.
[Л.Д.Гожая, 1988]

Таким образом, говоря о терминологии этой патологии, можно согласиться с компетентным мнением С.Т.Пыркова (1990), который считает, что при периодическом появлении патологических симптомов (кислый или металлический привкус по утрам или после приема кислой пищи, ощущение «прохождения» тока при введении металлических предметов в рот) целесообразно пользоваться термином «явления гальванизма», если же эти симптомы постоянны — «гальваноз». С.Т.Пырков считает, что при развитии аллергоза диагноз должен отражать клинический и патогенетический характер заболевания, например «аллергический катаральный стоматит, обусловленный никелем», а при клинической картине, характерной как для гальваноза, так и для аллергической реакции на металлы стоматологических реставраций, до установления этиопатогенеза заболевания или при отсутствии возможности его установить допускает использование термина «непереносимость».
Важно подчеркнуть, что патологический симптомокомплекс, характерный для явлений гальванизма или гальваноза, может развиваться при наличии в полости рта зубопротезных конструкций как из разнородных, так и из однородных сплавов металлов [Л.М.Детинич, 1967; Л.Д.Гожая, 1988 и др.].
Кроме того, такой симптомокомплекс может развиваться при нарушении технологии изготовления зубных протезов из нержавеющей стали или с покрытием нитрида титана, из-за нерационального использования припоя [Е.М.ТерПогосян, А.К.Иорданишвили, 1995]. Часто мы наблюдали явления гальванизма и гальванозы при наличии в полости рта больших паяных конструкций, особенно с острыми углами, что говорит о значении размеров и формы несъемных зубных протезов в возникновении этой патологии.
При наличии у больного явлений гальванизма (гальваноза) симптомокомплекс складывается из жалоб и объективных данных (местных и общих).
Обычно такие больные жалуются на появившийся после фиксации протезов металлический привкус, вкус соли, горечи или кислоты, который усиливается после приема кислой и соленой пищи, на жжение в полости рта, боль или жжение языка, обильное слюноотделение или сухость во рту, «чувство батарейки во рту», ощущение прохождения тока при введении в полость рта металлических предметов (особенно из алюминия), которые они образно характеризуют как «проскакивание искр в глазах», а также на головную боль, нарушение ночного сна, общую слабость, обострение хронических заболеваний желудочно-кишечного тракта, реже — патологические симптомы со стороны сердечно-сосудистой системы.
Е.В.Еричев, Т.П.Старченко, А.П.Стариков, С.Д.Гришечкин и А.Г.Захаркин (2001) проследили отдаленные результаты влияния металлов зубных протезов на ротовую жидкость у больных язвенной болезнью двенадцатиперстной кишки и установили, что таким больным категорически не показаны металлические зубные протезы из нержавеющей стали, так как наряду с возникающими субьективными ощущениями (привкус металла, ощущение кислоты) наблюдается достоверное увеличение объема секрета (58,3% больных) на 15,5% и снижение рН на 8,1%.
При осмотре полости рта чаще выявляют незначительную гиперемию слизистой оболочки полости рта в области протезного поля, появление на ней высыпных элементов, характерных для красного плоского лишая, реже — лейкоплакии, нарушение саливации (чаще — гиперсаливация). Слюна часто молочного цвета, пенистая. Язык обычно покрыт налетом, отечен, что легко диагностируется по отпечаткам зубов, имеющихся на его боковых поверхностях.
Такие больные раздражительны, мнительны, страдают канцерофобией, что говорит об изменении их психического и неврологического статуса.
Причем указанные симптомы встречаются как при низких (
< 5 мкА), средних (5-25 мкА), так и при высоких (>
30 мкА) значениях силы тока при его измерении между металлическими включениями в полости рта, между последними и слизистой оболочкой полости рта. «Повреждающей» величины микротоков в полости рта не обнаружено.
А.И.Воложин и С.Т.Пырков (1990), проводя глубокий анализ отечественной и зарубежной литературы по этому вопросу, отметили, что некоторые авторы в качестве физиологически переносимой называют разность потенциалов не более 50-80 мВ, но не обосновывают эти величины.
G.K.Fallschluessel (1986) считает, что по величинам потенциалов металлических включений, измеренных относительно различных электродов сравнения, вообще нереально судить об имеющемся коррозионном процессе. Измерение же потенциалов металлических протезов и определение напряжения между ними считают малоинформативными [H.Meiners, 1987]. В исследовании G.Hampf, A.Ekholm, T.Salo и др. (1987) не обнаружено статистических различий при измерении микротоков, потенциалов и энергоемкости зубных металлических протезов у здоровых и имеющих гальваноз. Использование методики регистрации потенциала каждого из металлических протезов с электродом сравнения и измерения поляризации разных поверхностей зубных протезов (косвенный метод подсчета микротоков по M.Bergmann, 1978) также не выявило статистически достоверных различий в величинах микротоков у здоровых и больных с гальванозом.
Поэтому электрические величины — сила тока, разность потенциалов между металлическими протезами и электродный потенциал металлической конструкции, измеренный относительно электрода сравнения, — малоинформативны [А.И.Воложин, С.Т.Пырков, 1990].
Небезосновательно мнение Visser, что при измерении в полости рта силы тока и напряжения с помощью обычных приборов в большинстве случаев регистрируется так называемый ток короткого замыкания, который возникает самостоятельно только в процессе измерения. Его временной график, кроме прочего, зависит от типа измерительного прибора. Поэтому, по мнению автора, электрические величины зависят прежде всего от процесса измерения, и проблема заключается не столько в сборе каких-либо показателей, сколько в доказательности этих данных с учетом примененного метода.
Установлено, что применяемые в исследованиях большинством авторов простые и легко осуществимые прямые методы измерений силы тока или разности потенциалов грешат малой точностью получаемых данных. Более точным является метод определения электродвижущих сил (ЭДС) гальванических элементов с помощью компенсационного метода, который заключается в том, что изучаемый гальванический элемент замыкают на внешнюю ЭДС, которую можно изменять и измерять. При этом их ЭДС направлены навстречу друг другу. Когда в измерительной цепи нет тока (стрелка гальваномера на нуле), ЭДС изучаемого гальванического элемента равна внешней ЭДС. Поскольку последняя вырабатывается источником тока, ее легко измерить с большой точностью [К.Б.Карандеев, 1963 и др.].
В то же время общим недостатком прямых и компенсационного методов является необходимость измерения электрических величин в каждой паре гальванических элементов. Это приводит, например, к тому, что при наличии в полости рта 20-25 металлических включений необходимо произвести 190-300 измерений [АН.Губская, В.С.Онищенко, 1974].
Результаты исследований АН.Губской и В.С.Онищенко (1974) показали, что даже точные измерения ЭДС, разности потенциалов или силы тока позволяют судить лишь о взаимодействии металлических включений между собой и не характеризуют величину потенциала каждого металлического включения в отдельности, что затрудняет определение наиболее электроактивных металлических включений, что имеет решающее значение при проведении лечебных мероприятий. Поэтому для диагностики гальваноза эти авторы предложили следующую методику. Обследование состоит из двух частей: изучения гальванических элементов и определения реакции слизистой оболочки на проходящий постоянный ток.
Первая часть исследования основана на принципе определения потенциалов отдельных гальванических полуэлементов. Для этого измеряют ЭДС гальванического элемента, образованного электродом сравнения, имеющего постоянный и устойчивый потенциал, и металлическим включением полости рта с помощью электроизмерительного прибора (мультоскоп Улибо рН-340) и электрода сравнения — хлорсеребряный ЭВЛ- 1-М2 с вмонтированным электролитическим ключом и отводящий игольчатый электрод конструкции авторов.
Конец электролитического ключа опускают на дно полости рта в слюну, а игольчатый электрод поочередно прикладывают к металлическим включениям, находящимся выше уровня слюны, и фиксируют показания. Отсчет величины потенциалов ведут по водородной шкале. Зная величину потенциала одного полуэлемента (электрод сравнения) и величину измеренной ЭДС, определяют потенциал другого полуэлемента (металлического включения). Таким образом устанавливают величину потенциала каждого металлического включения. По величине потенциалов все металлические включения полости рта располагаются в определенной последовательности, образуя своеобразный «ряд активности». Этот момент имеет, по мнению АН.Губской и В.С.Онищенко (1974), большое значение для последующей работы и является основным звеном предложенной им методики. Исходя из «ряда активности», без измерения определяют величину ЭДС между любыми металлическими включениями. Наибольшую величину ЭДС определяют по разнице или сумме (в зависимости от знака зарядов) потенциалов металлических включений, стоящих по краям «ряда активности». Между этими же включениями с помощью микроамперметра однократно измеряют величину силы тока, поскольку между ними чаще всего и определяется ее наибольшая величина 1. Эта величина необходима в дальнейшем для оценки влияния взаимодействия металлических включений на слизистую оболочку. Для более четкого представления о происходящих физико-химических процессах авторы методики рекомендуют также учитывать реакцию слюны (рН), так как она является одним из основных электролитных факторов, влияющих наэлектрические величины гальванических элементов.
А.В.Цимбалистов (1996) выявил закономерности в изменении концентрации веществ низкой и средней молекулярной массы (ВНиСММ) и олигопептидов (ОП) в крови, моче и слюне при физиологических и патологических состояниях организма и обосновал информативность и надежность ряда выбранных им показателей при использовании для оценки эндотоксикозов, вызываемых конструкционными материалами.
Известно, что метаболический статус ВНиСММ и ОП поддерживается в организме достаточно жестко. Эти показатели характеризуют прежде всего взаимоотношения организма и его адаптацию к условиям внешней среды. Наиболее стабильными являются концентрации ВНиСММ и ОП плазмы крови. В случае острой патологии, сопровождаемой активацией процессов метаболизма, оба показателя возрастают, а при хронизации патологии на фоне гипометаболизма — становятся ниже физиологических значений, что и позволяет считать эти показатели маркерами эндогенной интоксикации [М.Я.Малахова, С.В.Оболенский, 1989].
Особое значение для клиники ортопедической стоматологии придается коэффициенту моча/слюна содержания ВНиСММ и коэффициенту элиминации ВНиСММ.
Так, например, А.В.Цимбалистовым (1996) установлено, что при протезировании золотом по коэффициенту моча/слюна содержание ВНиСММ выглядит значительно лучше, чем при использовании КХС и стали с напылением нитрид титана, а наиболее близкий к норме коэффициент элиминации ВНиСММ выявлен также у людей, протезированных золотом. При использовании КХС последний показатель увеличивается, а при использовании стали с напылением нитрид титана накопление преобладает над выделением, что говорит об эндогенной интоксикации.
Важно подчеркнуть, что развитие синдрома эндогенной интоксикации возникает тем быстрее, чем несовершеннее системы и органы детоксикации: печень, почки, ЖКТ, легкие [А.В.Цимбалистов, 1996]. Это согласуется с ранее имевшимся мнением по этому вопросу [К.В.Темирова, Е.М.Тер-Погосян, 1977 и др.], а также данными по структуре соматической заболеваемости у больных с явлениями непереносимости зубных протезов [А.К.Иорданишвили, 1988, 1994].
Таким образом, А.В.Цимбалистов (1996), применив методику по исследованию эндотоксикоза как неизбежного элемента экзотоксикоза, разработал принципиально новый подход не только к оценке токсических качеств стоматологических конструкционных материалов, но и метаболического статуса организма и его адаптационного ресурса.
Склоняясь к мнению, что чувствительность к микротокам в полости рта индивидуальна, и убедившись в том, что дети менее чувствительны к микротокам в полости рта, мы не пренебрегаем использованием методики АН.Губской и соавт. (1974) в повседневной клинической практике. Такой методдиагностики часто помогал нам выбрать наиболее «активную» пару металлических включений в полости рта, элиминация одной из них в ряде случаев существенно улучшала самочувствие больных и снижала интенсивность неприятных ощущений в полости рта.
Лечение явлений гальванизма и гальваноза в полости рта предусматривает устранение конструкций из разнородных металлов и применение металлокерамических, цельнолитых или бесприпойных (лазерная сварка) протезов, их золочения, иногда протезов из сплавов благородных металлов при тщательном их полировании. Наилучший лечебный эффект дает использование протезов из ситалла, безметалловой керамики или пластмассы. В тех случаях, когда после удаления из полости рта металлических включений у больных продолжительное время сохраняются жалобы, то эффективно применение методов неспецифической терапии: ГБО, лазеротерапия, магнитотерапия, иглорефлексотерапия и др. [Е.М.Тер-Погосян и соавт., 1986-1991].
Профилактика явлений гальванизма и гальваноза сводится к соблюдению технологии изготовления зубных протезов, использованию современных методик их изготовления, что позволяет повысить индифферентность зубопротезных конструкций.
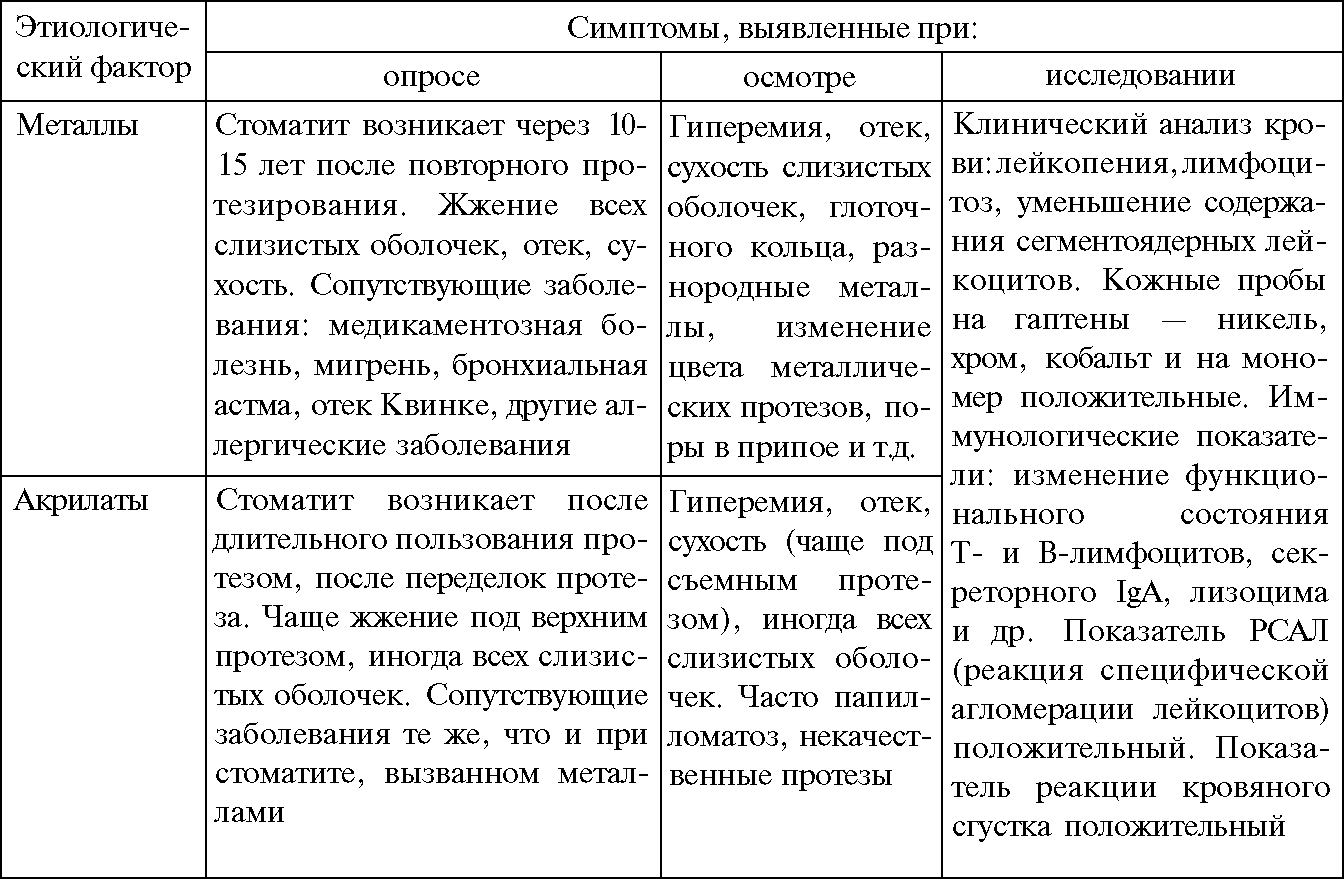
Данные о клинической картине симптомов аллергического стоматита представлены в табл. 21. В дополнение к сведениям Л.Д.Гожей (1988) отметим, что при аллергических стоматитах, обусловленных зубным протезом, больные также часто жалуются на металлический привкус, ощущение кислоты, жжение в полости рта, а также бессонницу, стомалгии и лицевые боли, обострение хронических заболеваний внутренних органов и систем организма. При осмотре полости рта могут определяться петехиальные кровоизлияния на слизистой оболочке твердого и мягкого неба, щек. Слюна тягучая, реже пенистая. Часто выявляются высыпные элементы красного плоского лишая. Также определяются функциональные нарушения со стороны нервной системы.
Д.Л.Демнер (1988) описывает менее выраженные проявления аллергического стоматита: легкая гиперемия слизистой оболочки протезного поля металлических протезов. Редко диагностируются внеротовые проявления аллергии в виде дерматита или их сочетание.
Описаны аллергические реакции на сплавы как из неблагородных, так и благородных металлов, используемых для изготовления зубных протезов, а также на никелево-титановую ортодонтическую проволоку (при содержании в ней Ni более 50%) и проволоку из нержавеющей стали.
Для диагностики аллергической природы заболевания часто используют на кожные капельные, компрессные или скарификационные пробы со стандартными аллергенами (0,5% р-р бихромата К, 2% р-р хлорида Со; 1% р-р хлорида Pd в вазелине, сульфат Ni в вазелине, а также 5% р-р хлорида Ni, 5% р-р нитрата Со на 60% этиловом спирте).
Симптомы аллергического стоматита (Л.Д.Гожая, 1988)
Метод внутриротовой пробы с образцами стоматологических материалов, описанный J.P.Morfi (1977), получил широкое практическое применение. Для его реализации созданы специальные устройства [И.Г.Иванченко, 1978; А.В.Цимбалистов и соавт., 1997].
В то же время положительный результат эпикутанной пробы к какому-либо аллергену еще не означает, что имеющиеся у пациента жалобы и клинические симптомы заболевания обусловлены аллергией.
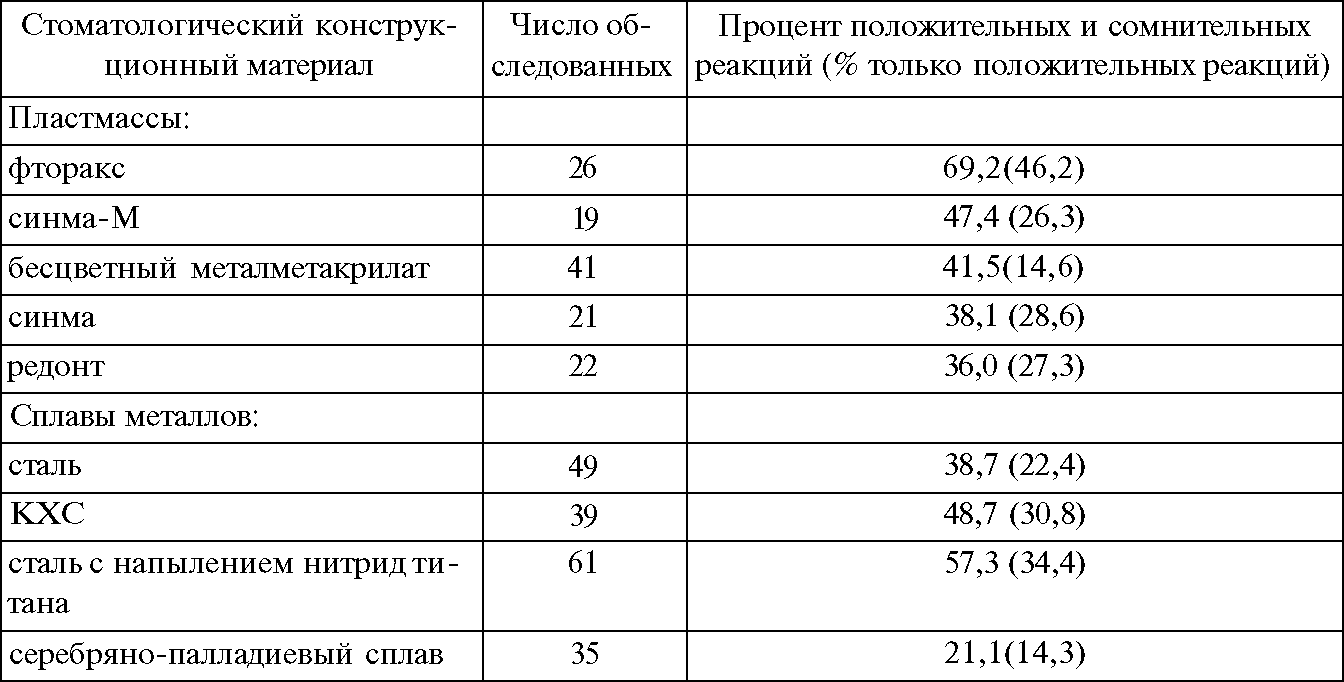
Приведем результаты накожно-аппликационных проб у пациентов к современным стоматологическим материалам (табл. 22).
Лечение аллергических стоматитов, обусловленных сплавами металлов ортопедических зубных конструкций, сводится к удалению из полости рта «причинных» реставраций и повторного протезирования с использованием индифферентных материалов.
По вопросу о профилактике аллергических стоматитов существуют противоположные мнения.
W.Rohrborn, K.Rork (1988) считают эпикутанное тестирование на этапе подготовки к зубному протезированию нецелесообразным из-за редкой встречаемости аллергических реакций, а также из-за возможности сенсибилизации больных во время этих процедур.
Д.Л.Демнер (1988) рекомендует проводить аллергологическое обследование у людей группы риска (1 — больные с анацидным гастритом, аллергическими
Таблица 21
Частота положительных и сомнительных реакций кожных проб пациентов с непереносимостью акриловых пластмасс и металлических сплавов [А.В.Цимбалистов, 1996]
заболеваниями, вегетососудистой дистонией; 2 — женщины 40-60 лет, повторно или дополнительно протезирующиеся, особенно при дисфункции яичников в предклимактерическом и климактерическом периоде; 3 — люди, отмечающие преходящие изменения вкуса при пользовании металлическими зубными протезами, которые возникают по утрам и во время приема кислой и острой пищи; 4 — люди, ощущающие дискомфорт при контакте с металлами на производстве и в быту в виде отека мочек ушной раковины при ношении металлических серег, так называемые тяжесть или зуд под цепочками или кольцами, появление удушья при наличии металлической пыли).
Мы придерживаемся второй точки зрения и рекомендуем проводить профилактические накожные аллергологические пробы с компонентами зубопротезных материалов у пациентов группы риска, в которую включаем людей пожилого и старческого возраста с хроническими заболеваниями ЖКТ, печени, болезнями крови с частыми обострениями, эндокринной патологией и аллергическими заболеваниями и у повторно протезируемых пациентов — людей, имеющих синдром непереносимости зубных протезов в анамнезе [К.В.Темирова, Е.М.Тер-Погосян, А.К.Иорданишвили, 1986]. Выполнять такие пробы и oceществлять их оценку должны только врачи-аллергологи, имеющие соответствующий сертификат, подтверждающий их профессиональную компетентность.
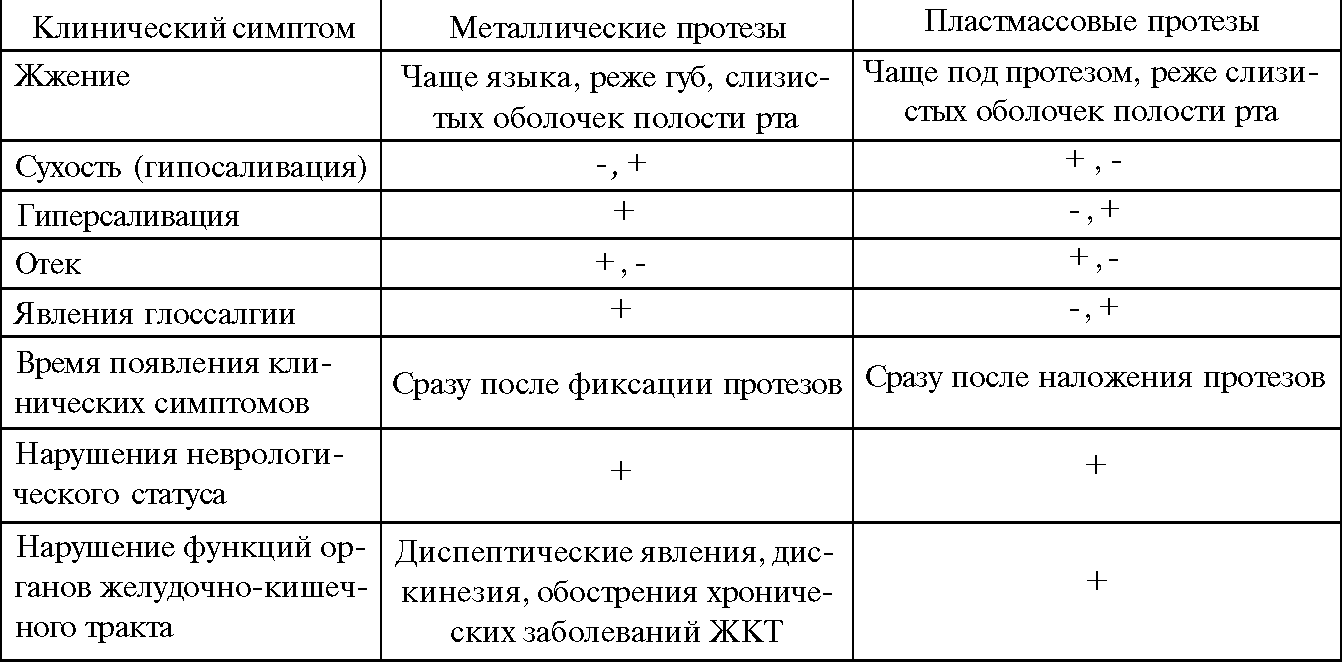
Материалы зубных протезов, особенно соединения тяжелых металлов, могут обусловливать токсические поражения организма, механизм которых складывается из местного и резорбтивного действия. Местно возникают токсические стоматиты (табл. 23). Кроме того, в слюне больных токсическим стоматитом, особенно при использовании протезов из нержавеющей стали, в 2-3 раза возрастает содержание микроэлементов: железа, серебра, никеля, свинца, хрома, олова, меди и др. При коррозии серебряно-палладиевых и золотых сплавов в слюне может увеличиваться содержание кадмия. Л.Д. Гожая (1988) установила прямую зависимость между качественным составом, количественным содержанием микроэлементов слюны и клиникой токсических реакций, а также показала, что спектрограмма слюны является тестом объективной и достоверной оценки электрохимических процессов в полости рта. Одновременно возможно увеличение содержания микроэлементов в желудочном соке, крови, моче и слизистой оболочке полости рта.
Таблица 22
В диагностике токсических поражений, обусловленных металлическими включениями в полости рта, также помогает определение рН слюны, показатель которого сдвигается в кислую сторону, измерение разности потенциалов (микротоков), которая увеличивается. Возможны изменения в крови в виде увеличенной СОЭ, лейкоцитоза, эритропении, уменьшения количества гемоглобина.
Таблица 23
Клиника токсико-химического стоматита, возникшего под действием материала _ протеза (Л.Д.Гожая, 1988)_
Лечение токсических поражений сводится к удалению из полости рта причинных ортопедических конструкций, элиминирующей терапии и повторного протезирования индифферентными материалами.
В заключение отметим, что дифференциальная диагностика указанных заболеваний крайне сложна даже для врачей-стоматологов с большим профессиональным опытом и стажем работы, требует тщательного комплексного обследования с обязательным привлечением врачей-интернистов.